【題目】Ⅰ:可逆反應(yīng)在某體積為5L的密閉容器中進(jìn)行����,在從0﹣3分鐘各物質(zhì)的量的變化情況如圖所示(A��,B����,C均為氣體)
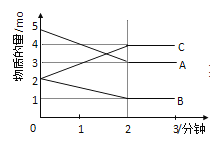
(1)該反應(yīng)的化學(xué)方程式為______________;
(2)恒溫恒容下��,N2(g)+3H2(g)  2NH3(g),達(dá)到平衡的標(biāo)志有_______________��。
2NH3(g),達(dá)到平衡的標(biāo)志有_______________��。
A.3v正(H2)=2v逆(NH3)
B.混合氣體總質(zhì)量不在隨時(shí)間變化
C.容器內(nèi)的壓強(qiáng)不再隨時(shí)間而變化
D. N2���、H2�、NH3的濃度之比為1:2:3
E.單位時(shí)間生成nmolN2�����,同時(shí)消耗3nmolH2
F.?dāng)嚅_一個(gè)N≡N鍵的同時(shí)有6個(gè)N—H鍵生成
Ⅱ:以氨作為燃料的燃料電池����,具有能量效率高的特點(diǎn),另外氨氣含氫量高���,易液化��,方便運(yùn)輸和貯存���,是很好的氫源載體。燃料電池的結(jié)構(gòu)如圖所示:
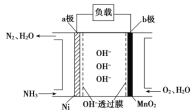
①a極是電池的______________(填“正”或“負(fù)”)極�����,電極反應(yīng)式為________________。
②當(dāng)生成0.5molN2時(shí)�����,電路中通過的電子的物質(zhì)的量為_____�����。
Ⅲ:甲醇水蒸氣重整制氫方法是目前比較成熟的制氫方法��,且具有良好的應(yīng)用前景�����。甲醇水蒸氣重整制氫的部分反應(yīng)過程如圖所示:
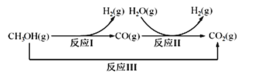
(1)已知一定條件下
反應(yīng)I: CH3OH(g)=CO(g)+2H2(g) ΔH1=+90.7kJ/mol
反應(yīng)III:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH3=+49.5kJ/mol
該條件下反應(yīng)II的熱化學(xué)方程式是____________________________��。
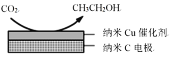
(2)如圖����,酸性電解質(zhì)溶液中����,電解CO2可以制備乙醇,寫出陰極的電極方程式:____________________________����。