
科目: 來(lái)源: 題型:

查看答案和解析>>
科目: 來(lái)源: 題型:
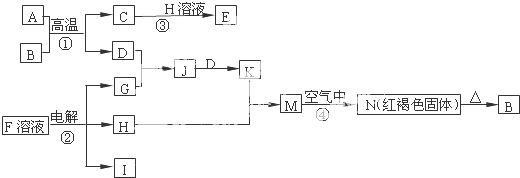
查看答案和解析>>
科目: 來(lái)源: 題型:

查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
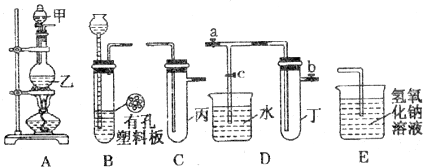
| 實(shí)驗(yàn)序號(hào) | 實(shí)驗(yàn)操作 | 現(xiàn)象 | 結(jié)論 |
| Ⅰ | 將氯水滴入品紅溶液 | 品紅溶液褪色 | 氯氣與水反應(yīng)的產(chǎn)物有漂白性 |
| Ⅱ | 氯水中加入碳酸氫鈉粉末 | 有無(wú)色氣泡產(chǎn)生 | 氯氣與水反應(yīng)的產(chǎn)物具有酸性 |

查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
| 物質(zhì) | Al | Fe2O3 | Al2O3 | Fe |
| 熔點(diǎn)(℃) | 660 | 1462 | 2054 | 1535 |
| 沸點(diǎn)(℃) | 2467 | - | 2980 | 2750 |
| 所用試劑 | |
| 實(shí)驗(yàn)操作及現(xiàn)象 | |
| 有關(guān)反應(yīng)的化學(xué)方程式 |
查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
科目: 來(lái)源: 題型:
 合成氨對(duì)農(nóng)業(yè)生產(chǎn)及國(guó)防建設(shè)均具有重要意義.
合成氨對(duì)農(nóng)業(yè)生產(chǎn)及國(guó)防建設(shè)均具有重要意義.查看答案和解析>>
科目: 來(lái)源: 題型:
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com