���P(gu��n)��(x��)�}
0 5309 5317 5323 5327 5333 5335 5339 5345 5347 5353 5359 5363 5365 5369 5375 5377 5383 5387 5389 5393 5395 5399 5401 5403 5404 5405 5407 5408 5409 5411 5413 5417 5419 5423 5425 5429 5435 5437 5443 5447 5449 5453 5459 5465 5467 5473 5477 5479 5485 5489 5495 5503 203614
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
���з���(y��ng)���x�ӷ���ʽ���_����
- A.
���ˮ�еμ�FeCl
3��Һ�Ƃ�Fe��OH��
3�z�w��Fe
3++3H
2O

Fe��OH��
3��+3H
+ - B.
��С�K���ί�θ���^(gu��)�ࣺNaHCO3-+H+=Na++CO2��+H2O
- C.
��(sh��)�(y��n)�����}���cMnO
2����(y��ng)��Cl
2��MnO
2+4H
++2Cl
-
Cl
2��+Mn
2++2H
2O
- D.
��FeCl3��Һ���gӡˢ�·�壺Fe3++Cu=Fe2++Cu2+
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
���з���(y��ng)����Ԫ��ȫ����߀ԭ����
- A.
MnO
2+4HCl���⣩

MnCl
2+2H
2O+Cl
2��
- B.
Cl2+2NaOH=NaCl+NaClO+H2O
- C.
5Cl2+I2+6H2O=10HCl+2HIO3
- D.
Cu��OH��2+2HCl�TCuCl2+2 H2O
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ�����}
��18mol/L ����������100ml 3.0mol/L ϡ����Č�(sh��)�(y��n)�� �ش����І�(w��n)�}��
��1�������������w�e��______mL������һλС��(sh��)������
��2���F(xi��n)�����ЎNҎ(gu��)��ăx�����������(y��ng)�x��______
��10mL��Ͳ�� ��50mL��Ͳ�� ��100mL��Ͳ�� ��100mL����ƿ�� ��250mL����
��3�����ԓ��(sh��)�(y��n)߀��Ҫ�ăx����______
��4��ijͬ�W(xu��)�����õĝ����ᾏ������ʢ���m�����sˮ�ğ�����ϡ��������������?c��i)��������s��ֱ�ӵ��M(j��n)���x���ҽ�(j��ng)�z�鲻©ˮ������ƿ�У�ϴ�����2-3��������ϴ��ҺҲ��������ƿ������΄�(d��ng)����ƿʹ���Ͼ��������Ȼ���ˮ���x�̶Ⱦ�2cm̎��������õιܼ�ˮ���̶Ⱦ���������ԇ��ƿ�N�Ϙ�(bi��o)�����ã�Ո(q��ng)ָ�����������еă�̎���@�e(cu��)�`��
��______
��______
��5��������r��(du��)�����Ƶ�ϡ�������к�Ӱ�����������ƫ����ƫС���o(w��)Ӱ푡���
�����õĝ������L(zh��ng)�r(sh��)�g�������ܷⲻ�õ����������______
����ȡ������r(sh��)��ҕ��Ͳ�̶Ⱦ���______
������ƿ�����sˮϴ���](m��i)������_(k��i)ʼ��Һ����______
�ܶ��ݕr(sh��)��ҕ����ƿ�̶Ⱦ�����______��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ�����}
������һ�K�c¶���ڿ՚���һ�Εr(sh��)�g�������������������҃�λͬ�W(xu��)�ѹ��w�ֳɃɷݣ���ȡһ��ͬ�r(sh��)�M(j��n)�Ќ�(sh��)�(y��n)������̽����M�ɺͺ�����Ո(q��ng)����(j��)Ҫ��ش����І�(w��n)�}��
��ͬ�W(xu��)����һ�ݷ����ƿ�������������ϡ��������������ɟo(w��)ɫ�o(w��)ζ�Ě��w����(j��)�������������ж�����̼�͚�������Ȼ���M(j��n)�К��w�ɷݵ��(y��n)�C��(sh��)�(y��n)��
��1�����(y��n)�C���w�a(ch��n)�����Ƿ��ж�����̼�͚���������D���x���Ҫ�ăx����ˎƷ�������O(sh��)Ӌ(j��)һ���b���(y��n)�C���w�ɷݣ��b�õ��B�����?y��n)�?br/>d��______��______��______��______��______��______���������b�õĽӿ���ĸ��
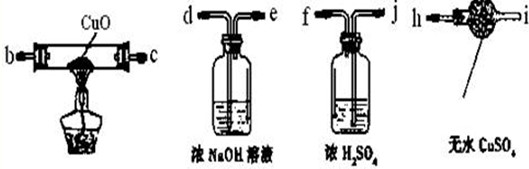
��2����(sh��)�(y��n)�^(gu��)�����^�쵽ʯ��ˮ׃���ᣬ�ɴ˿��Д�ԭ���w�к��е����|(zh��)��______����W(xu��)ʽ����
��ͬ�W(xu��)����һ���M(j��n)������(sh��)�(y��n)��
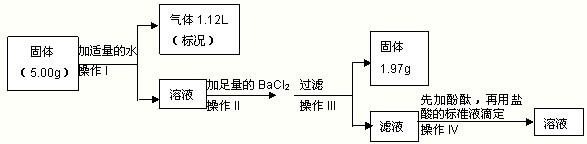
��3���Ý��}������500mL 3.00mol?L-1��ϡ�}��r(sh��)�����Ҫʹ�õIJ����x��������Ͳ������������z�^�ιܡ����������⣬߀��______��
��4���ڲ���II����������l(f��)������(y��ng)���x�ӷ���ʽ��_(k��i)_____��
��5������IV�����}���(bi��o)��(zh��n)Һ�ζ��VҺ�r(sh��)����ζ��K�c(di��n)�ĬF(xi��n)����______��
��6��������IV�У�����3.00mol?L-1���}���(bi��o)��(zh��n)Һ50.00mL����ͨ�^(gu��)Ӌ(j��)���Д��������5.00g���w���Ƿ���NaOH______�����л�o(w��)�������|(zh��)����______g�������J(r��n)��o(w��)NaOH����t�˿ղ��ô𣩣�
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
ͬ��ͬ���£�ij������MO2��116g��������MCO2��122g������F(xi��n)��Mij���w��114g��������tij���w�ķ�������
- A.
28
- B.
60
- C.
32
- D.
4
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
���Ќ�(sh��)�(y��n)�����O(sh��)Ӌ(j��)�����������е���
- A.
��O2��H2�Ļ�Ϛ��wͨ�^(gu��)�Ɵ�������~���Գ�ȥ���е�H2
- B.
����ȡ�ķ������x���ͺ�ú��
- C.
���ܽ���^(gu��)�V�ķ������x����⛺��Ȼ��c���w�����
- D.
��ϡ�}����^(gu��)�V�����ȥ�����~���е������V�ۺ��F��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ�����}
�����f(shu��)����������_����________
A�����^(gu��)�����A�ğ����͈A�ן�ƿ���������Ȼ�̼��������c��Һϴ��
B������(sh��)�(y��n)�r(sh��)������ֱ����ȡ�����c
C�����бP��ƽ�Q��50.56gKCl
D����ú�Ϳ��ԏ�͵�ˮ����ȡ��
E��һ����ͨ�^(gu��)�z�w���Ĵ�ֱ�ڹ⾀�ķ�����Կ���һ�l�����ġ�ͨ·��
F���ĺ��������Ȼ��c���������Һ����ȡ����⛿��ýY(ji��)���ķ���
G���õ��۵⻯�ԇ��ȥ�z�(y��n)��Һ���Ƿ������������|(zh��)���������_�������������sˮ��(r��n)��ԇ������������ճ�ڲ�����һ���������Ȼ��ԇ��������Һ����������ԇ���ɫ�Ƿ�׃�{(l��n)��
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
���г��s���x�õ�ԇ��������������ȫ���_��һ�M��
| �x�(xi��ng) | ���ἃ�����|(zh��) | �x�õ�ԇ�� | �������� |
| A | NaCl��NH4Cl�� | - | �ӟ� |
| B | CO2��CO�� | CuO | ϴ�� |
| C | CO2��SO2�� | �С�K����Һ | ϴ�� |
| D | NaCl��Һ��Na2SO4�� | BaCl2��Һ | �^(gu��)�V |
- A.
A
- B.
B
- C.
C
- D.
D
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ����x�}
��(sh��)�(y��n)�����Ȼ��@����ʯ���ư�����b�ú������ķN�ƚ��b����ͬ
- A.
�ӟ���i�����O2
- B.
ʯ��ʯ��ϡ�}�ᷴ��(y��ng)��CO2
- C.
MnO2���^(gu��)��������Һ�ֽ���O2
- D.
MnO2�c��HCl�ӟ���ȡ�Ț�
�鿴�𰸺ͽ���>>
��Ŀ��
��(l��i)Դ��
�}�ͣ�����}
���I(y��)�����S�F�V��ԭ�����a(ch��n)������Ҫ�֞�����(g��)�A���M(j��n)�У����џ������������������գ�Ո(q��ng)�ش����Ђ�(g��)��(w��n)�}��
��1���џ��S�F�V�γɵĠt���횽�(j��ng)���m�����ϴ���������������M(j��n)��______�����O(sh��)�����Q�����������ҪĿ����______��
��2����������ʹ�õĴ����C�|ý��V2O5���ܼӿ���������������ʣ����^(gu��)���Юa(ch��n)����һ�B�������g�w����D1��������a���c�����Ļ��W(xu��)����ʽ�ɱ�ʾ�飺______��______��
��3��550��r(sh��)�����SO2�D(zhu��n)����SO3��ƽ���D(zhu��n)���ʣ������c�wϵ������(qi��ng)��p�����P(gu��n)ϵ��D2��ʾ���t����2.0mol SO2��1.0mol O2����5L���]�����������������(y��ng)�_(d��)ƽ��������wϵ������(qi��ng)��0.10M Pa��ԓ����(y��ng)��ƽ�ⳣ��(sh��)����______��A�cB��ʾ��ͬ����(qi��ng)�µ�SO2�D(zhu��n)�������ͨ����r�¹��I(y��)���a(ch��n)�в��ó�����ԭ����______��
��4����ѭ�h(hu��n)���ô��������������ˆT����������һ�N�x�ӽ��Q�������C���¹�ˇ��
�������_(d��)91.7%���ϣ���֪�U�C�����к���V2O5�����VOSO4�������Ԛ�?ji��n)�������Y��֪��VOSO4������ˮ�����V2O5�y����ˮ������NH4VO3�y����ˮ��ԓ��ˇ��������D��
�t������(y��ng)�٢ڢۢ��Ќ�������߀ԭ����(y��ng)����______���(sh��)����̖(h��o)���������(y��ng)�ٵ��x�ӷ���ʽ��_(k��i)_____��ԓ��ˇ�з���(y��ng)�۵ij����ʣ��ַQ���\�ʣ��ǻ����C���P(gu��n)�I֮һ�����C�ʵĸߵͳ�����ҺpHӰ���������߀��Ҫ�����Ȼ��@ϵ��(sh��)��NH4Cl�����|(zh��)���c��Һ��V2O5���|(zh��)���ȣ��͜ضȣ�����(j��)�Dԇ���h�����Ȼ��@ϵ��(sh��)�Ͷȣ�______��______��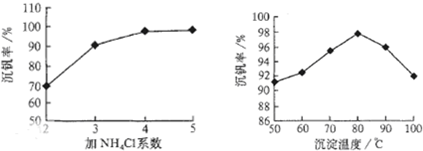
�鿴�𰸺ͽ���>>

 Fe��OH��3��+3H+
Fe��OH��3��+3H+ Cl2��+Mn2++2H2O
Cl2��+Mn2++2H2O MnCl2+2H2O+Cl2��
MnCl2+2H2O+Cl2��



