
題目列表(包括答案和解析)
已知下列熱化學(xué)反應(yīng)方程式:
①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
②Fe2O3(s)+1/3CO(g)===2/3Fe3O4(s)+1/3CO2(g) ΔH=-15.73 kJ/mol
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
則14gCO氣體還原足量FeO固體得到固體Fe和CO2氣體時(shí)對(duì)應(yīng)的ΔH為
已知下列熱化學(xué)反應(yīng)方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)
ΔH=-24.8 kJ/mol
Fe2O3(s)+![]() CO(g)===
CO(g)===![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g)
CO2(g)
ΔH=-15.73 kJ/mol
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g)
ΔH=+640.4 kJ/mol
則14 g CO氣體還原足量FeO固體得到Fe固體和CO2氣體時(shí)對(duì)應(yīng)的ΔH約為( )
A.-218 kJ/mol B.-109 kJ/mol
C.+218 kJ/mol D.+109 kJ/mol
已知下列熱化學(xué)反應(yīng)方程式:
①Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
②Fe2O3(s)+1/3CO(g)===2/3Fe3O4(s)+1/3CO2(g) ΔH=-15.73 kJ/mol
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
則14 g CO氣體還原足量FeO固體得到固體Fe和CO2氣體時(shí)對(duì)應(yīng)的ΔH為
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
|
已知下列熱化學(xué)反應(yīng)方程式: Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8 kJ/mol Fe2O3(s)+2/3CO(g)=2/3Fe3O4(s)+1/3CO2(g)△H=-15.73 kJ/mol Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.4 kJ/mol 則14 g CO氣體還原足量FeO固體得到Fe固體和CO2氣體時(shí)對(duì)應(yīng)的△H約為 | |
| [ ] | |
A. |
-218 kJ/mol |
B. |
-109 kJ/mol |
C. |
+218 kJ/mol |
D. |
+109 kJ/mol |
已知下列熱化學(xué)反應(yīng)方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol①
Fe2O3(s)+ CO(g)=
CO(g)=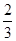 Fe3O4(s)+
Fe3O4(s)+ CO2(g) ΔH=-15.73 kJ/mol②
CO2(g) ΔH=-15.73 kJ/mol②
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol③
則14 g CO氣體還原足量FeO固體得到Fe固體和CO2氣體時(shí)對(duì)應(yīng)的ΔH約為( )
| A.-218 kJ/mol | B.-109 kJ/mol |
| C.+218 kJ/mol | D.+109 kJ/mol |
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com