
題目列表(包括答案和解析)
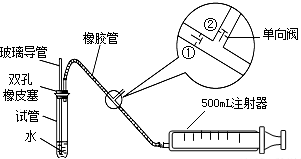
| 分組 | 第一小組 | 第二小組 |
| 抽氣時(shí)間 | 20分鐘 | 21分鐘 |
| 抽氣次數(shù) | 100 | 130 |
| SO2含量:mg/m3 |
| 分組 | 第一小組 | 第二小組 |
| 抽氣時(shí)間 | 20分鐘 | 21分鐘 |
| 抽氣次數(shù) | 100 | 130 |
| SO2含量:mg/m3 |
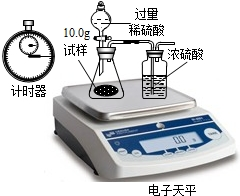
| 稱 量 項(xiàng) 目 | 稱 量 時(shí) 間 | 質(zhì)量(g) |
| 試樣 | 10.00 | |
| 裝置+稀硫酸質(zhì)量 | 241.30 | |
| 裝置+稀硫酸質(zhì)量+試樣 | 反應(yīng)開始后15秒 | 249.20 |
| 裝置+稀硫酸質(zhì)量+試樣 | 反應(yīng)開始后35秒 | 248.20 |
| 裝置+稀硫酸質(zhì)量+試樣 | 反應(yīng)開始后55秒 | 248.00 |
| ||
| ||
| 1 |
| 5 |
| 1 |
| 5 |
| ||
| ||
 | 配料表 |
| 摩擦劑:SiO2(20%) CaCO3(少量) 清潔劑:NaHCO3(15%) 發(fā)泡劑:K12(極少量) 保濕劑:甘油等(60%) 增稠劑:卡拉膠等 其他:香精、水等 |
| 實(shí)驗(yàn)編號 | 1 | 2 | 3 |
| 實(shí)驗(yàn)前(g) | 2.00 | 2.00 | 2.00 |
| 實(shí)驗(yàn)后(g) | 0.43 | 0.44 | 0.45 |
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com