
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}

≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
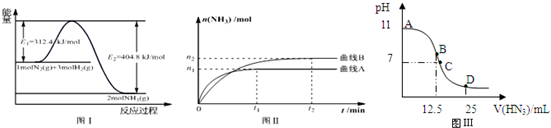
| úō∂»/°ś | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
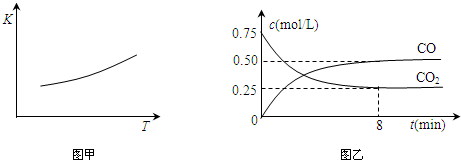
| ērťg/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c£®NO£©/mol•L-1 | 1.00°Ń10-3 | 4.50°Ń10-4 | 2.50°Ń10-4 | 1.50°Ń10-4 | 1.00°Ń10-4 | 1.00°Ń10-4 |
| c£®CO£©/mol•L-1 | 3.60°Ń10-3 | 3.05°Ń10-3 | 2.85°Ń10-3 | 2.75°Ń10-3 | 2.70°Ń10-3 | 2.70°Ń10-3 |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
 “‘Őž»Ľö‚ěť‘≠ŃŌļŌ≥…ľ◊īľ≥£“äĶń∑Ĺ∑®”–ňģ√ļö‚∑®ļÕńŅ«į’ż‘ŕť_įl(f®°)Ķń÷ĪĹ”—űĽĮ∑®£ģ
“‘Őž»Ľö‚ěť‘≠ŃŌļŌ≥…ľ◊īľ≥£“äĶń∑Ĺ∑®”–ňģ√ļö‚∑®ļÕńŅ«į’ż‘ŕť_įl(f®°)Ķń÷ĪĹ”—űĽĮ∑®£ģ≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļŖxďŮÓ}
| A£ģ | 20% | B£ģ | 25% | C£ģ | 33% | D£ģ | 50% |
≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}

≤ťŅīīūįłļÕĹ‚őŲ>>
Ņ∆ńŅ£ļ ĀŪ‘ī£ļ Ó}–Õ£ļĹ‚īūÓ}
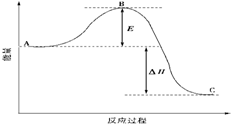 2SO2£®g£©+O2£®g£©?2SO3£®g£©∑īĎ™(y®©ng)Ŗ^≥ŐĶńń‹ŃŅ◊ÉĽĮ»ÁąDňý ĺ£ģ“—÷™1mol SO2£®g£©—űĽĮěť1mol SO3£®g£©Ķń°ųH=-99kJ•mol-1£ģ
2SO2£®g£©+O2£®g£©?2SO3£®g£©∑īĎ™(y®©ng)Ŗ^≥ŐĶńń‹ŃŅ◊ÉĽĮ»ÁąDňý ĺ£ģ“—÷™1mol SO2£®g£©—űĽĮěť1mol SO3£®g£©Ķń°ųH=-99kJ•mol-1£ģ≤ťŅīīūįłļÕĹ‚őŲ>>
įŔ∂»÷¬–Ň - ĺöŃēÉ‘Ń–ĪŪ - ‘áÓ}Ń–ĪŪ
ļĢĪĪ °Ľ•¬ď(li®Ęn)ĺW(w®£ng)Ŗ`∑®ļÕ≤ĽŃľ–ŇŌĘŇeąů∆ĹŇ_ | ĺW(w®£ng)…Ō”–ļ¶–ŇŌĘŇeąůĆ£Ö^(q®Ī) | Žä–Ň‘pÚ_ŇeąůĆ£Ö^(q®Ī) | …śöv ∑Őďüo÷ųŃx”–ļ¶–ŇŌĘŇeąůĆ£Ö^(q®Ī) | …ś∆ů«÷ôŗ(qu®Ęn)ŇeąůĆ£Ö^(q®Ī)
Ŗ`∑®ļÕ≤ĽŃľ–ŇŌĘŇeąůŽä‘í£ļ027-86699610 Ňeąůŗ]Ōš£ļ58377363@163.com