【題目】大氣中NOx�、SO2等污染物的有效去除和資源的充分利用是當(dāng)今社會的重要研究課題,目前采用的方法如下:
I.直接轉(zhuǎn)化法:利用高效催化劑將汽車尾氣直接轉(zhuǎn)化為無毒物質(zhì)��。
已知:N2(g)+O2(g)=2NO(g)△H1=+180kJ·mol-1
(1)利用固體表面催化工藝將NO分解為N2����、O2而消除污染。
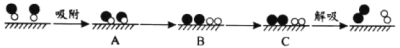
用 分別表示N2�����、NO、O2和固體催化劑�,在固體催化劑表面分解NO的過程如圖所示。從吸附到解吸的過程中����,能量狀態(tài)最低的是________________________(填字母序號)。
分別表示N2�����、NO、O2和固體催化劑�,在固體催化劑表面分解NO的過程如圖所示。從吸附到解吸的過程中����,能量狀態(tài)最低的是________________________(填字母序號)。
(2)利用稀土等催化劑能將汽車尾氣中的CO���、NO直接轉(zhuǎn)化成無毒物質(zhì)N2�����、CO2��。
①已知:C(s)�、CO(g)的燃燒熱分別為393kJ·mol-1�����、283kJ·mol-1���,寫出NO(g)與CO(g)催化轉(zhuǎn)化成N2(g)和CO2(g)的熱化學(xué)方程式________________________���。
②為研究上述反應(yīng),某學(xué)習(xí)小組在密閉容器中充入10molCO和10molNO��,發(fā)生上述①所寫反應(yīng)�����,實驗測得平衡時NO的體積分?jǐn)?shù)隨溫度��、壓強(qiáng)的關(guān)系如圖��。

a.某溫度下的平衡狀態(tài)D點(diǎn)����,若同時采取縮小容器體積和降低溫度,重新達(dá)到平衡狀態(tài)時��,可能到達(dá)圖中A~G點(diǎn)中的________________________點(diǎn)����。
b.當(dāng)壓強(qiáng)為10MPa、溫度為T時的平衡常數(shù)Kp=________________________(用平衡分壓代替平衡濃度計算�,分壓=總壓×物質(zhì)的量分?jǐn)?shù);保留3位有效數(shù)字)�。
II.催化還原法:利用還原劑在催化劑的作用下將氮氧化物轉(zhuǎn)為無毒物質(zhì)N2�、CO2���。
(3)用活性炭還原法可以處理汽車尾氣中的氮氧化物��。
某研究小組在2L的恒容密閉容器中加入一定量的NO和足量的固體活性炭�,發(fā)生反應(yīng):C(s)+2NO(g)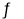 N2(g)+CO2(g)���。在不同溫度下測得平衡體系中各物質(zhì)的物質(zhì)的量如表:
N2(g)+CO2(g)���。在不同溫度下測得平衡體系中各物質(zhì)的物質(zhì)的量如表:
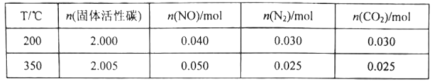
①該反應(yīng)的正反應(yīng)為________________________(填“吸熱”或“放熱”)反應(yīng)�����。
②350℃時��,反應(yīng)達(dá)到平衡后向恒容容器中再充入0.100molNO��,再次達(dá)到平衡后�����,N2的體積分?jǐn)?shù)應(yīng)為________________________�����。
A.0.5B.0.25C.介于0.25和0.5之間D.無法確定
III.電解法:利用電解的方法將氨氧化物轉(zhuǎn)化為有用物質(zhì)��,從而達(dá)到資源的回收利用�。
(4)如圖所示的電解裝置��,可將霧霾中的NO2��、SO2轉(zhuǎn)化為硫酸銨���,從而實現(xiàn)廢氣的回收再利用�����,回答下列問題:
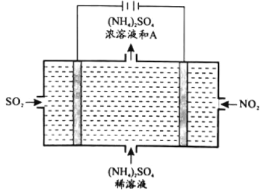
①陰極的電極反應(yīng)式為________________________��。
②上圖中A物質(zhì)是________________________�����。